Pilas de combustible I - Hidrógeno
Los primeros antecedentes de este ingenio humano, llamado “Pila de Combustible” datan del año 1838, fecha en la cual Christian Friederich Schoenbein, realizó los primeros experimentos con un electrolito ácido que generaba corriente eléctrica a partir de hidrógeno y oxígeno.
Historia del la Pila de Combustible
Los primeros antecedentes de este ingenio humano, llamado “Pila de Combustible” datan del año 1838, fecha en la cual Christian Friederich Schoenbein, realizó los primeros experimentos con un electrolito ácido que generaba corriente eléctrica a partir de hidrógeno y oxígeno. A partir de esta experiencia se generó el desarrollo de las llamadas Cell Fuel, cuyo real debut se produjo a principio de los años 60, cuando el programa espacial de la National Agency Space Administration (NASA), promovió el desarrollo de pilas de combustibles alcalinas (AFC), para abastecer de electricidad y agua a las naves espaciales Apollo y los cohetes Shuttle Orbiters. Por cierto era la manera más eficiente y silenciosa para abastecer a una nave espacial de electricidad, agua y calor con un reducido peso. Así en 1966, se construyó la primera pila de combustible de 1,5 kW para tres astronautas. Desde esa fecha todos los viajes espaciales han contado con pilas de combustible. Actualmente se incorporan 3 pilas de combustible por nave cada una de 7kW, con picks máximos de 12kW durante 15 minutos y eficiencia mayor al 70%. Dado que en el espacio no existe atmosfera el hidrógeno y oxígeno necesarios para el funcionamiento de la pila se almacenan bajo el muelle de carga de la nave.
Desde el año 2007, las pilas de combustible iniciaron su masificación para una variedad de aplicaciones que analizaremos en el desarrollo de estos artículos.
Actualmente las pilas de combustible o Fuel Cell, son usadas para energizar eléctricamente barcos, camiones, vehículos pequeños, montacargas, equipos mineros, plantas de generación eléctrica comunales y domiciliarias, etc. Esta tecnología es una solución no contaminante para aquellas localidades e instalaciones aisladas que carecen de red eléctrica tales como cuarteles militares y policiacos, instalaciones fronterizas, instalaciones antárticas, centros de producción aislados, centros de salud, escuelas, hogares etc.
¿Que es una pila de combustible?
Es un dispositivo electrónico que convierte directamente la energía química de un combustible en energía eléctrica en presencia de un oxidante (Oxigeno) Está formada por un conjunto de Celdas interconectadas entre sí. Una agrupación de estas celdas da origen al nombre de “Pila” Todas las CELDAS tienen tres componentes fundamentales: un electrodo poroso positivo o CATODO, un electrodo poroso negativo o ANODO y un ELECTROLITO que separa ambos electrodos y cuya función es facilitar el paso de ciertos iones y dificultar el paso de electrones por lo cual a este electrolito es dieléctrico.
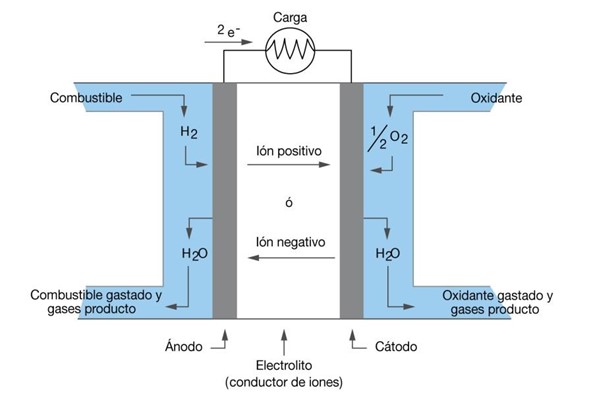
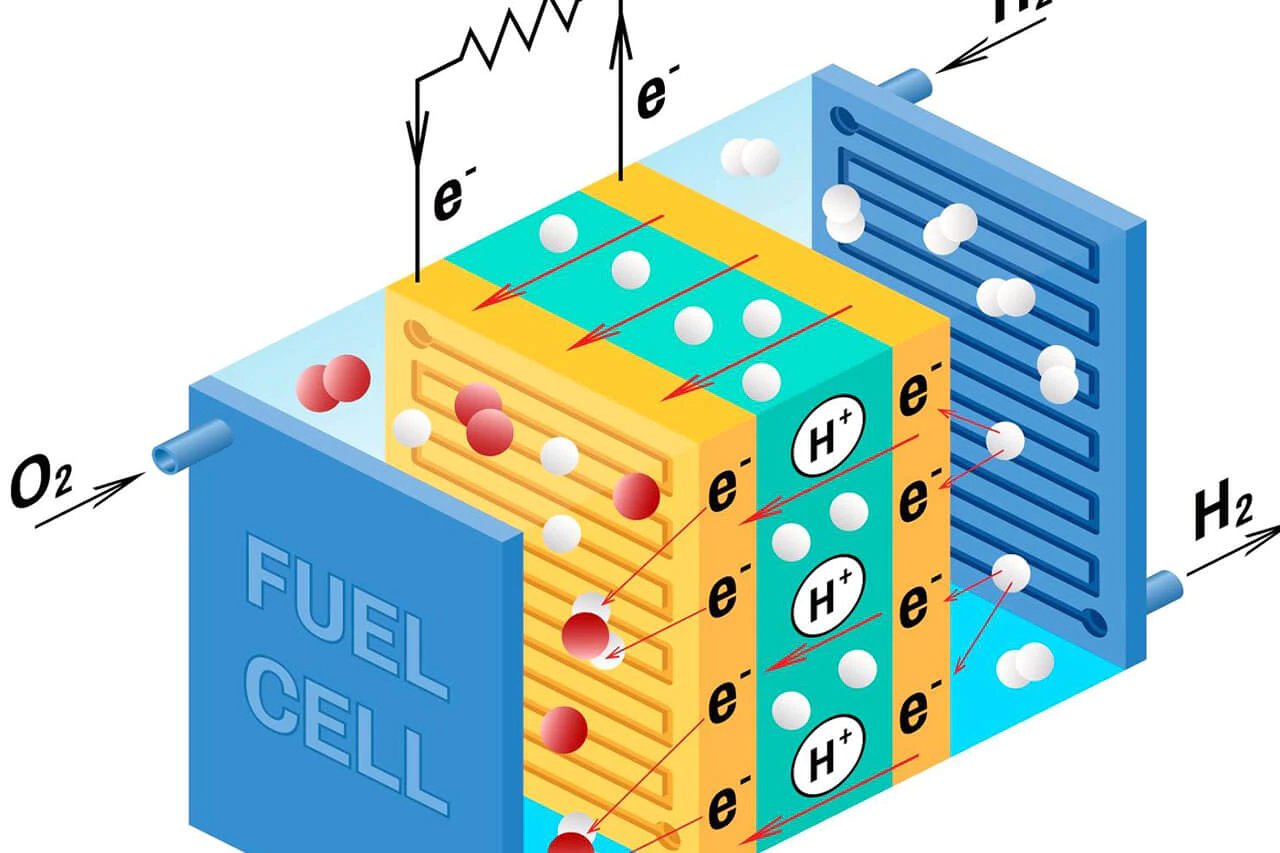
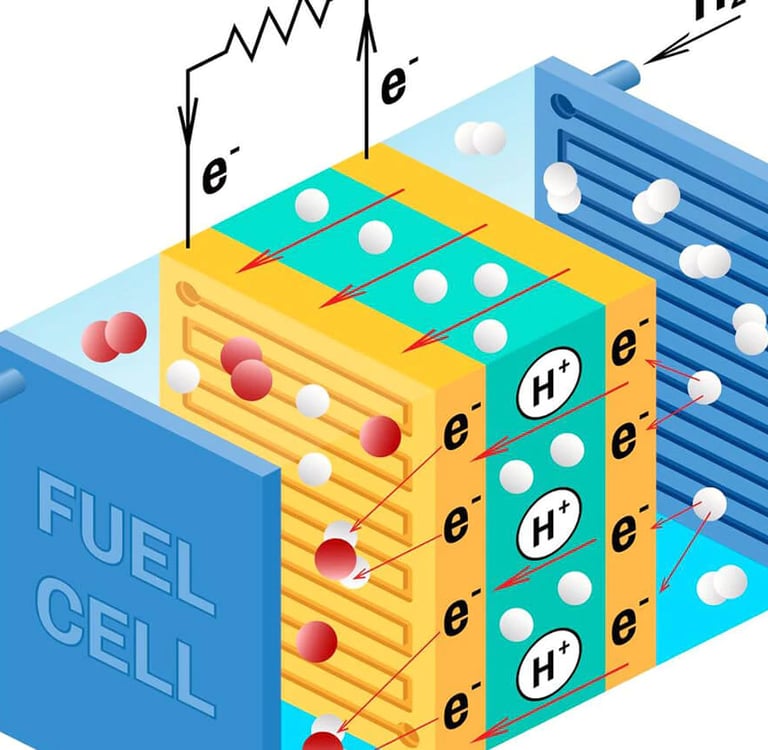
El ANODO, suministra el combustible, generalmente hidrógeno. Aquí se disocia la molécula de hidrógeno (H₂) en dos iones (protones H+) sobrando dos electrones (e⁻) punto 1 en Figura. 2.
El ELECTROLITO, deja pasar los protones (H+) pero no los electrones (e⁻). Punto 2 en figura 2.
El CATODO, suministra oxígeno (generalmente del ambiente). Éste disocia la molécula de oxígeno en iones O² (se requieren 2 electrones por ion) y se unen con los iones de H+ para formar moléculas de agua (H₂O). Punto 3 en figura 2.
Las reacciones de ánodo y cátodo generan un potencial electroquímico entre sí, que se manifiesta en un Voltaje Eléctrico.
Los electrones liberados en el ANODO, no pueden llegar al CATODO a través del electrolito que es dieléctrico, por lo que se requiere un circuito eléctrico externo entre ánodo y cátodo formando una corriente eléctrica útil.
ANODO+ ELECTROLITO + CÁTODO = AGUA + ELECTRICIDAD + CALOR.
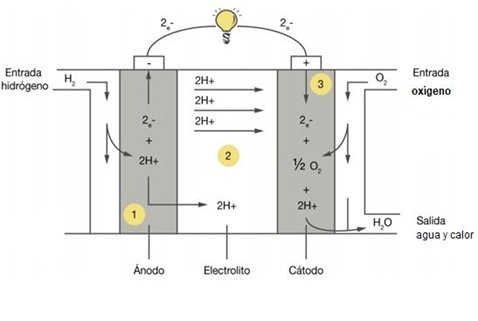

Figura N° 2 Movimiento de iones, electrones y protones en una celda de combustible.
En una pila de combustible son reactivos el HIDRÓGENO y OXÍGENO y los productos son agua y calor, no existen contaminantes en la producción de energía eléctrica.
¿Cuál es la diferencia entre una pila de combustible y una batería o alimentador electro químico?
Una Pila de Combustible se alimenta permanentemente de combustible ingresándolo al Ánodo, al mismo tiempo el suministro continuo de oxígeno al Cátodo, esto permite que este sistema puede funcionar permanentemente 7 x 24 y esa es la gran diferencia o ventaja con los alimentadores electroquímicos o baterías.
Por otra parte una batería es un dispositivo acumulador de energía y su máxima energía disponible está determinada por el reactante químico almacenado dentro de la misma batería, esto implica que un alimentador electro-químico dejará de producir energía eléctrica cuando se consuman los reactantes químicos (se descargue).
Una bateria almacena energía y necesita recarga
En una batería recargable los reactantes se regeneran por recargas lo cual supone introducir energía en la batería mediante una fuente externa.
Una pila de combustible alimentada externa y continuamente con los reactantes genera la energía en su interior.
Mientras una pila de combustible sea alimentada externamente con combustible entregará energía al usuario
Una pila de combustible genera energía y depende del abastecimiento externo de combustible (h₂)
El hidrógeno gaseoso es el combustible preferido pero no el único (metanol y etanol) para las Pilas de Combustible, esto gracias a que los productos de la reacción con hidrógeno no afectan el medio ambiente.
Por otra parte se han desarrollado combinaciones de sistemas que convierten gases o líquidos combustibles tales como el gas natural, derivados del petróleo, gas de síntesis, biogás, etc, a mezclas de gases inocuos con hidrógeno de alta pureza. Sin embargo todos los sistemas generados a partir de hidrocarburos tienen efectos nocivos en el medio ambiente.
El diseño de una pila de combustible considera la tensión de trabajo y corriente demandada, a partir de las cuales se diseña el número de celdas de combustible y el área activa de cada una de ellas.


